幽门螺杆菌(Helicobacter pylori,Hp)是一种螺旋形、专性微需氧、对生长条件要求十分苛刻的细菌。1983年首次从慢性活动性胃炎患者的胃黏膜活检组织中成功分离,它是目前所知唯一能在人胃中长期生存的微生物。
1994年,世界卫生组织(WHO)的国际癌症研究机构(International agency for research on cancer, IARC)将幽门螺杆菌定为胃癌的Ⅰ类致癌物,它也因此成为世界上第一个被正式认可的可致癌的细菌。
(1)HP重要研究事件

(2)HP的致病性
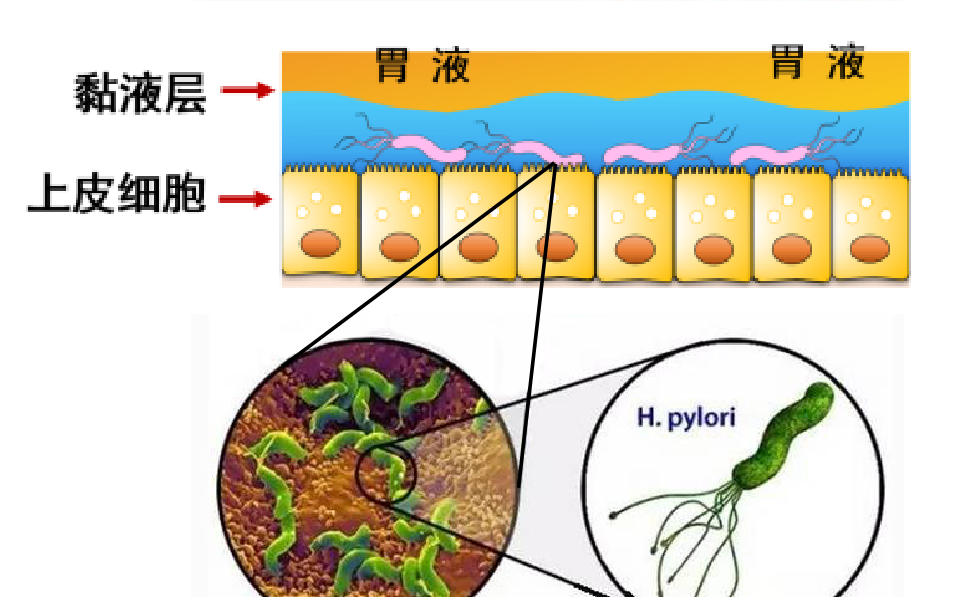
通常Hp在胃黏膜上皮细胞的表面呈不均匀团状分布,也可穿过上皮细胞,进入到黏膜层,并且由于其自身特有的“S”型菌体形状以及鞭毛,使其能够在粘稠液体中快速游动。Hp还能借助多种黏附因子与特异性受体牢固结合。因此,Hp能长期寄居于胃黏膜上皮细胞,也能自由穿梭于黏液层,并且长期寄居胃黏膜深层,从而引起一系列的炎症或疾病。
Hp首先分泌尿素酶,尿素酶分解以后能够产生微量的尿素,尿素再次分解后产生的氨能够中和胃酸,形成使Hp能够抵御高胃酸环境的保护膜。然后,Hp会分泌多种毒素(细胞空泡毒素、细胞毒素相关蛋白等)以及多种酶(热休克蛋白、过氧化氢酶、蛋白水解酶等),这些毒素以及酶使其能够损伤胃黏膜上皮细胞。同时Hp还会分泌抑制胃酸的蛋白,影响胃酸的形成。
(3)HP的致病因子
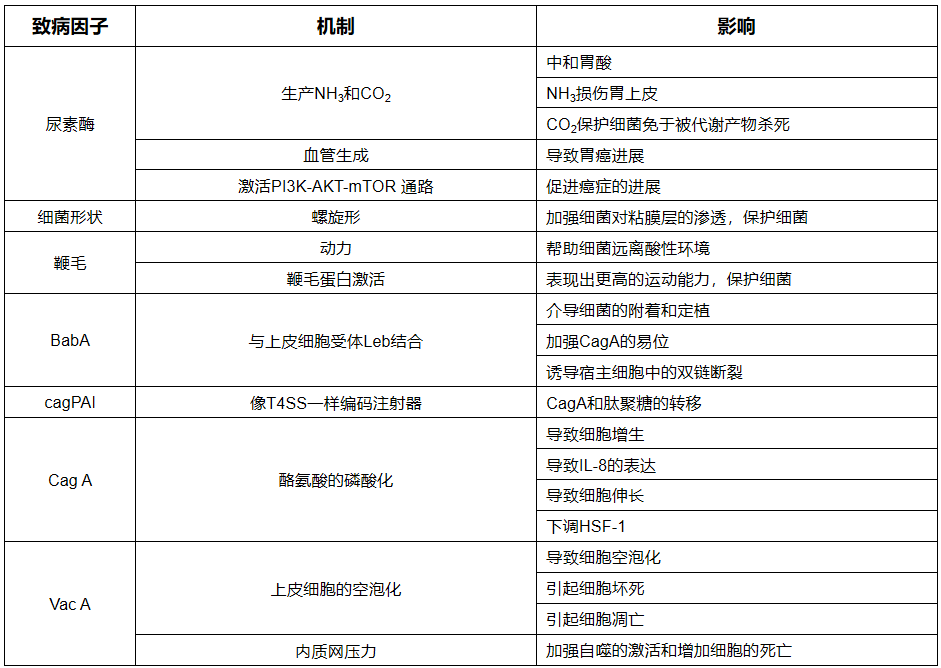
Hp具有多种致病因子,包括尿素酶、Cag A以及Vac A等。在胃上皮细胞表面定植是其致病的先决条件,因此,其中最关键的就是尿素酶的分泌。尿素酶分解尿素产生的氨不仅可以破坏胃酸环境,使其酸性变弱,从而使细菌能够抵御胃酸,同时还能对上皮细胞起到一定的损伤作用。研究显示,尿素酶的活性与胃黏膜上皮细胞的凋亡呈正相关。Cag A和Vac A是两个主要的毒力因子,也可能是胃癌发生的始动因素。
(4)Hp感染病程进展
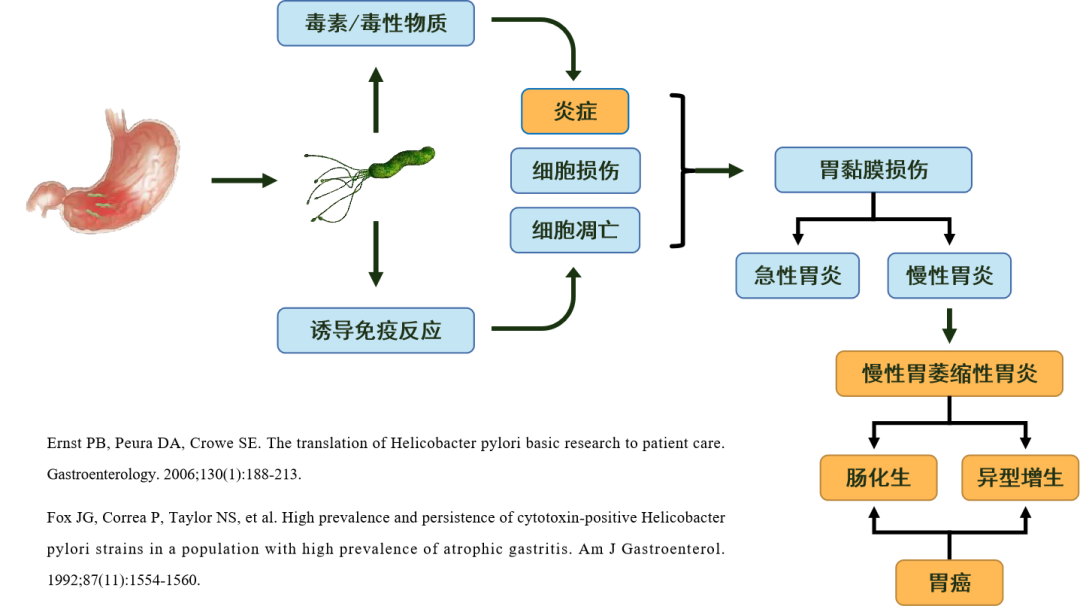
Hp感染后,通过其致病因子的作用直接损伤胃粘膜上皮细胞,诱导免疫反应,从而造成胃黏膜炎症。
Hp感染诱导的免疫反应难以将Hp清除,感染持续,导致长期慢性感染。慢性感染引起的胃黏膜慢性炎症(慢性浅表性胃炎)是Hp感染引起相关疾病的基础病变。
胃黏膜慢性炎症可导致慢性胃萎缩性胃炎的发生,在Hp的作用下,破坏胃黏膜的保护屏障,长期的破坏、修复、再破坏,使上皮细胞反复损伤并引起严重的炎症反应,以致逐渐出现肠上皮化生和异型增生等细胞病理变化。胃黏膜上皮细胞发生癌前病变,最终导致胃癌的发生。
据调查,正常人群中Hp阳性率约50%,感染Hp的患者中没有明显症状的感染者占15%,转化为胃癌的概率达1%。并且随着抗生素的广泛使用,Hp的耐药性越来越高,根除率也越来越低,严重威胁公众的健康安全。因此,了解幽门螺杆菌,提高预防幽门螺杆菌感染的健康意识十分重要!
 站内搜索
站内搜索